|
Поделиться ссылкой:
Прочитать статью в pdf формате Хронический некалькулезный холецистит - это воспалительное заболевание, вызывающее поражение стенки желчного пузыря и моторно-тонические нарушения билиарной системы, которое проявляется болью билиарного типа (1). Причиной моторной дисфункции желчного пузыря может выступать сужение пузырного протока, мышечная гипертрофия, хроническое воспаление стенки желчного пузыря.
Диагностические критерии хронического некалькулезного холецистита
- Повторяющиеся эпизоды умеренной или тяжелой боли, локализованной в эпигастрии или правом подреберье и продолжающиеся в течение многих часов. Боли возникают и усиливаются после приема жирной и жареной пищи, яиц, холодных газированных напитков, вина, пива, острых продуктов.
- Кроме того, боль может сочетаться с одним и более из следующих признаков:
- Тошнота, рвота, постоянное чувство тяжести в верхних отделах живота
- Отрыжка, вздутие живота
- Возникновение боли после приема пищи
- Возникновение боли в ночное время
- Нарушение эвакуаторной функции желчного пузыря.
- По данным УЗИ исследования утолщение стенки желчного пузыря до 3-4 мм.
Причины болевого синдрома, хронического воспаления в стенке и нарушения эвакуаторной функции желчного пузыря
- Патология гладкомышечных и эпителиальных клеток желчного пузыря (повышенная экспрессия ЦОГ-2 в гладкомышечных и эпителиальных клетках стенки желчного пузыря).
- Дискоординация желчного пузыря и пузырного протока (повышенная экспрессия ЦОГ-2 в гладкомышечных клетках желчного пузыря и пузырного протока).
- Увеличение сопротивление пузырного протока (повышенная экспрессия ЦОГ-2 в гладкомышечных клетках пузырного протока).
Механизм развития патологических нарушений
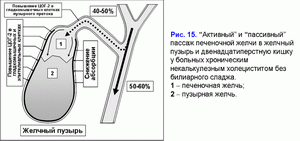
Повышенная экспрессия ЦОГ-2 в гладкомышечных клетках стенки желчного пузыря способствует снижению эвакуаторной функции желчного пузыря и “активного” пассажа печеночной желчи в желчный пузырь (рис. 15).
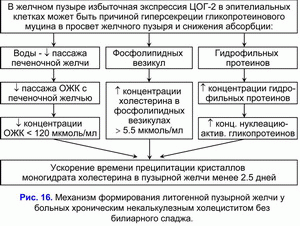
Повышенная экспрессия ЦОГ-2 в эпителиальных клетках стенки желчного пузыря способствует снижению абсорбционной функции желчного пузыря (уменьшение абсорбции воды и билиарного холестерина в фосфолипидных везикулах) и “пассивного” пассажа печеночной желчи в желчный пузырь. Это сопровождается уменьшением концентрации общих желчных кислот в пузырной желчи и увеличением концентрации билиарного холестерина в фосфолипидных везикулах и способствует нарушению коллоидной стабильности пузырной желчи и преципитации гранул билирубината кальция и кристаллов моногидрата холестерина, т.е. формированию “литогенной” пузырной желчи (рис. 16). Повышенная экспрессия ЦОГ-2 в эпителиальных клетках стенки желчного пузыря способствует гиперсекреции гликопротеинового муцина в просвет желчного пузыря и пузырную желчь. Увеличение концентрации гликопротеинового муцина сопровождается повышением вязкости пузырной желчи.
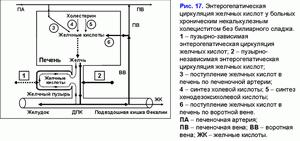
Снижение “активного” и “пассивного” пассажа печеночной желчи в желчный пузырь способствует увеличению пассажа печеночной желчи в двенадцатиперстную кишку и пузырно-независимой энтерогепатической циркуляции желчных кислот, билиарного холестерина и билирубина (рис. 17).
Увеличению пузырно-независимой энтерогепатической циркуляции желчных кислот способствует увеличению концентрации желчных кислот в гепатоцитах и снижению накопительно-выделительной функции печени (т.е. формированию хронического “мягкого” внутрипеченочного холестаза) (рис. 17).
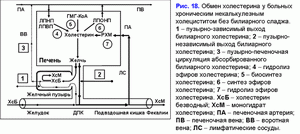
Увеличению пузырно-независимой энтерогепатической циркуляции билиарного холестерина способствует увеличению абсорбции билиарного холестерина в тонкой кишке, поступлению билиарного холестерина в гепатоциты и повышенной секреции в печеночную желчь (рис. 18).
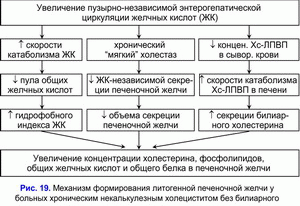
Эти два фактора способствуют формированию “литогенной” печеночной желчи (рис. 19).
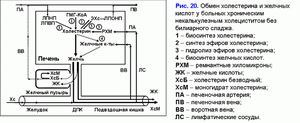
Снижение пузырно-зависимого выведения билиарного холестерина и уменьшение концентрации желчных кислот в пузырной желчи способствуют формированию “литогенной” пузырной желчи и преципитации кристаллов моногидрата холестерина в просвете желчного пузыря у 40% больных хроническим некалькулезным холециститом без билиарного сладжа (рис. 20).
Избыточная экспрессия активности ЦОГ-2 в эпителиальных клетках слизистой желчного пузыря способствует гиперсекреции гликопротеинового муцина в пузырную желчь. Повышение концентрации гликопротеинового муцина в пузырной желчи более 2 мг/мл вызывает его полимеризацию и формирование участков повышенной вязкости. Преципитация кристаллов моногидрата холестерина и гранул билирубината кальция в полимеризованных участках гликопротеинового муцина способствует формированию билиарного сладжа и трансформации хронического некалькулезного холецистита без билиарного сладжа в хронический некалькулезный холецистит с билиарного сладжа.
Патогенетическое лечение больных хроническим некалькулезным
холециститом без билиарного сладжа
Соответственно, лечение хронического некалькулезного холецистита без билиарного сладжа (с болевым синдромом) и с целью профилактики хронического некалькулезного холецистита с билиарным сладжем, дуоденограстрального рефлюкса, атрофического гастрита антрального отдела желудка и хронического билиарного панкреатита включает:
- Целекоксиб - по 100 мг 2 раза в день после еды - 5-7 дней, после чего
- Урсодезоксихолевая кислота - по 750 мг 1 раз в день на ночь - 1 месяц.
Целекоксиб - селективный ингибитор ЦОГ-2, ингибируя активность ЦОГ-2 в гладкомышечных клетках стенки желчного пузыря и пузырного протока, способствует устранению болевого синдрома в течение 3-5 дней, восстановлению эвакуаторной функции желчного пузыря и пузырно-зависимого выведения билиарного холестерина, “активного” и “пассивного” пассажа печеночной желчи в желчный пузырь и снижению пузырно-независимой энтерогепатической циркуляции желчных кислот, билиарного холестерина и билирубина.
Целекоксиб - селективный ингибитор ЦОГ-2, ингибируя активность ЦОГ-2 в эпителиальных клетках стенки желчного пузыря, способствует снижению секреции гликопротеинового муцина в просвет желчного пузыря, концентрации гликопротеинового муцина в пузырной желчи и вязкости пузырной желчи, что предупреждает формирование билиарного сладжа. Сниженная активность ЦОГ-2 в эпителиальных клетках стенки желчного пузыря помогает восстанавливать абсорбционную функцию желчного пузыря (абсорбцию воды и билиарного холестерина из фосфолипидных везикул, что способствует увеличению концентрации желчных кислот и уменьшению концентрации билиарного холестерина в пузырной желчи.
Урсодезоксихолевая кислота - гидрофильная гепатозащитная желчная кислота способствует растворению кристаллов моногидрата холестерина в желчном пузыре, снижению литогенности пузырной и печеночной желчи, разрешению хронического “мягкого” внутрипеченочного холестаза (т.е. способствует восстановлению накопительно-выделительной функции печени).
Целекоксиб - селективный ингибитор ЦОГ-2, ингибируя активность ЦОГ-2 в гладкомышечных клетках желчевыводящих протоков и сфинктера Одди, способствует устранению болевого синдрома в течение 3-5 дней и восстановлению пассажа печеночной желчи в двенадцатиперстную кишку.
Целекоксиб - селективный ингибитор ЦОГ-2, ингибируя активность ЦОГ-2 в эпителиальных клетках желчевыводящих протоков, способствует снижению секреции гликопротеинового муцина в просвет желчевыводящих протоков, концентрации гликопротеинового муцина в печеночной желчи и вязкости печеночной желчи, что предупреждает формирование билиарного сладжа и желчных камней в желчевыводящих протоках.
Сниженная активность ЦОГ-2 в эпителиальных и гладкомышечных клетках желчевыводящих протоков помогает уменьшить риск развития холедохолитиаза.
Урсодезоксихолевая кислота - гидрофильная гепатозащитная желчная кислота способствует растворению кристаллов моногидрата холестерина в желчевыводящих протоках, снижению литогенности печеночной желчи, разрешению хронического “мягкого” внутрипеченочного холестаза (т.е. способствует восстановлению накопительно-выделительной функции печени) и у части больных способствует растворению билиарного сладжа в желчевыводящих протоках (1-66).
Урсодезоксихолевая кислота - гидрофильная гепатозащитная желчная кислота, снижая агрессивные свойства желчи, препятствует развитию хронического атрофического гастрита антрального отдела желудка (дуоденограстральный рефлюкс, реактивный гастрит или желчный гастрит), хронического билиарного панкреатита (билиопанкреатический рефлюкс) и хронического спаситического панкреатита (III панкреатический тип дисфункции сфинктера Одди) (1-66).
Целекоксиб и Урсодезоксихолевая кислота, патогенетически блокируя основные механизмы образования желчных камней, способствуют профилактике образования желчных камней в желчевыводящих протоках и снижают риск развития холедохолитиаза и билиарного панкреатита (1-66).
Эффективность - 95%.
Продолжительность ремиссии - 18-24 месяца.
Внимание!!! Информация для больных:
Перед использованием данной схемы лечения убедительная просьба посмотреть противопоказания (см. ниже) и побочные эффекты при применении фармакологических препаратов целекоксиба и урсодезоксихолевой кислоты и получить разрешение у вашего лечащего врача.
Противопоказания для применения целекоксиба:
- аллергические реакции (крапивница, бронхоспазм) на прием ацетилсалициловой кислоты или других НПВС (в анамнезе);
- III триместр беременности;
- известная повышенная чувствительность к сульфонамидам;
- повышенная чувствительность к любому компоненту препарата.
Противопоказания для применения урсодезоксихолевой кислоты:
- повышенная чувствительность к препарату;
- острые воспалительные заболевания желчного пузыря и желчных протоков;
- неспецифический язвенный колит;
- болезнь Крона.
Сайт не несет юридической ответственности за использование представленных схем лечения без согласования с лечащим врачом.
Список литературы:
-
Практикующий врач: гастроэнтерология. 2002; 1: 22.
Список литературы (Целекоксиб (Celecoxib) и Урсодезоксихолевая кислота (Ursodeoxycholic Acid)):
- Chen XW, Cai JT. The impact of selective cycloxygenase-2 inhibitor celexibo on the formation of cholesterol gallstone. Zhonghua Nei Ke Za Zhi. 2003; 42(11): 797-9.
- Tomida S, Abei M, Yamaguchi T, Matsuzaki Y, Shoda J, Tanaka N, Osuga T. Long-term ursodeoxycholic acid therapy is associated with reduced risk of biliary pain and acute cholecystitis in patients with gallbladder stones: a cohort analysis. Hepatology. 1999; 30(1): 6-13.
- Carotti S, Guarino MP, Cicala M, Perrone G, Alloni R, Segreto F, Rabitti C, Morini S. Effect of ursodeoxycholic acid on inflammatory infiltrate in gallbladder muscle of cholesterol gallstone patients. Neurogastroenterol Motil. 2010.
- Guarino MP, Carotti S, Morini S, Perrone G, Behar J, Altomare A, Alloni R, Caviglia R, Emerenziani S, Rabitti C, Cicala M. Decreased number of activated macrophages in gallbladder muscle layer of cholesterol gallstone patients following ursodeoxycholic acid. Gut. 2008; 57(12): 1740-1.
- Guarino MP, Carotti S, Sarzano M, Alloni R, Vanni M, Grosso M, Sironi G, Maffettone PL, Cicala M. Short-term ursodeoxycholic acid treatment improves gallbladder bile turnover in gallstone patients: a randomized trial. Neurogastroenterol Motil. 2005; 17(5): 680-6.
- Pazzi P, Petroni ML, Prandini N, Adam JA, Gullini S, Northfield TC, Jazrawi RP. Postprandial refilling and turnover: specific gallbladder motor function defects in patients with gallstone recurrence. Eur J Gastroenterol Hepatol. 2000; 12(7): 787-94.
- Jazrawi RP, Pazzi P, Petroni ML, Prandini N, Paul C, Adam JA, Gullini S, Northfield TC. Postprandial gallbladder motor function: refilling and turnover of bile in health and in cholelithiasis. Gastroenterology. 1995; 109(2): 582-91.
- Ikegami T, Matsuzaki Y, Fukushima S, Shoda J, Olivier JL, Bouscarel B, Tanaka N. Suppressive effect of ursodeoxycholic acid on type IIA phospholipase A2 expression in HepG2 cells. Hepatology. 2005; 41(4): 896-905.
- Shoda J, Ueda T, Kawamoto T, Todoroki T, Asano T, Sugimoto Y, Ichikawa A, Maruyama T, Nimura Y, Tanaka N. Prostaglandin E receptors in bile ducts of hepatolithiasis patients and the pathobiological significance for cholangitis. Clin Gastroenterol Hepatol. 2003; 1(4): 285-96.
- Tazuma S, Nishioka T, Ochi H, Hyogo H, Sunami Y, Nakai K, Tsuboi K, Asamoto Y, Sakomoto M, Numata Y, Kanno K, Yamaguchi A, Kobuke T, Komichi D, Nonaka Y, Chayama K. Impaired gallbladder mucosal function in aged gallstone patients suppresses gallstone recurrence after successful extracorporeal shockwave lithotripsy. J Gastroenterol Hepatol. 2003; 18(2): 157-61.
- Shoda J, Kano M, Asano T, Irimura T, Ueda T, Iwasaki R, Furukawa M, Kamiya J, Nimura Y, Todoroki T, Matsuzaki Y, Tanaka N. Secretory low-molecular-weight phospholipases A2 and their specific receptor in bile ducts of patients with intrahepatic calculi: factors of chronic proliferative cholangitis. Hepatology. 1999; 29(4): 1026-36.
- Kano M, Shoda J, Irimura T, Ueda T, Iwasaki R, Urasaki T, Kawauchi Y, Asano T, Matsuzaki Y, Tanaka N. Effects of long-term ursodeoxycholate administration on expression levels of secretory low-molecular-weight phospholipases A2 and mucin genes in gallbladders and biliary composition in patients with multiple cholesterol stones. Hepatology. 1998; 28(2): 302-13.
- Shoda J, Ueda T, Ikegami T, Matsuzaki Y, Satoh S, Kano M, Matsuura K, Tanaka N. Increased biliary group II phospholipase A2 and altered gallbladder bile in patients with multiple cholesterol stones. Gastroenterology. 1997; 112(6): 2036-47.
- Sasaki H, Tazuma S, Kajiyama G. Effects of 16,16-dimethyl prostaglandin E2 on biliary mucous glycoprotein and gallstone formation in guinea pigs. Scand J Gastroenterol. 1993; 28(6): 495-9.
- Mizuno S, Tazuma S, Kajiyama G. Stabilization of biliary lipid particles by ursodeoxycholic acid. Prolonged nucleation time in human gallbladder bile. Dig Dis Sci. 1993; 38(4): 684-93.
- Tazuma S, Sasaki H, Mizuno S, Sagawa H, Hashiba S, Horiuchi I, Kajiyama G. Effect of ursodeoxycholic acid administration on nucleation time in human gallbladder bile. Gastroenterology. 1989; 97(1): 173-8.
- Jüngst C, Sreejayan N, Zündt B, Müller I, Spelsberg FW, Hüttl TP, Kullak-Ublick GA, del Pozo R, Jüngst D, von Ritter C. Ursodeoxycholic acid reduces lipid peroxidation and mucin secretagogue activity in gallbladder bile of patients with cholesterol gallstones. Eur J Clin Invest. 2008; 38(9): 634-9.
- Jüngst C, Sreejayan N, Eder MI, von Stillfried N, Zündt B, Spelsberg FW, Kullak-Ublick GA, Jüngst D, von Ritter C. Lipid peroxidation and mucin secretagogue activity in bile of gallstone patients. Eur J Clin Invest. 2007; 37(9): 731-6.
- Fischer S, Müller I, Zündt BZ, Jüngst C, Meyer G, Jüngst D. Ursodeoxycholic acid decreases viscosity and sedimentable fractions of gallbladder bile in patients with cholesterol gallstones. Eur J Gastroenterol Hepatol. 2004; 16(3): 305-11.
- Sauter GH, Thiessen K, Parhofer KG, Jüngst C, Fischer S, Jüngst D. Effects of ursodeoxycholic acid on synthesis of cholesterol and bile acids in healthy subjects. Digestion. 2004; 70(2): 79-83.
- Wang DQ, Tazuma S. Effect of beta-muricholic acid on the prevention and dissolution of cholesterol gallstones in C57L/J mice. J Lipid Res. 2002; 43(11): 1960-8.
- Fromm H, Malavolti M. Bile acid dissolution therapy of gallbladder stones. Baillieres Clin Gastroenterol. 1992; 6(4): 689-95.
- Sunami Y, Tazuma S, Kajiyama G. Gallbladder dysfunction enhances physical density but not biochemical metastability of biliary vesicles. Dig Dis Sci. 2000; 45(12): 2382-91.
- Nishioka T, Tazuma S, Yamashita G, Kajiyama G. Partial replacement of bile salts causes marked changes of cholesterol crystallization in supersaturated model bile systems. Biochem J. 1999; 340 (Pt 2): 445-51.
- Fahey DA, Carey MC, Donovan JM. Bile acid/phosphatidylcholine interactions in mixed monomolecular layers: differences in condensation effects but not interfacial orientation between hydrophobic and hydrophilic bile acid species. Biochemistry. 1995; 34(34): 10886-97.
- Guarino MP, Cong P, Cicala M, Alloni R, Carotti S, Behar J. Ursodeoxycholic acid improves muscle contractility and inflammation in symptomatic gallbladders with cholesterol gallstones. Gut. 2007; 56(6): 815-20.
- Mas MR, Comert B, Mas N, Yamanel L, Ozotuk H, Tasci I, Jazrawi RP. Effects of long term hydrophilic bile acid therapy on in vitro contraction of gallbladder muscle strips in patients with cholesterol gallstones. World J Gastroenterol. 2007; 13(32): 4336-9.
- Colecchia A, Mazzella G, Sandri L, Azzaroli F, Magliuolo M, Simoni P, Bacchi-Reggiani ML, Roda E, Festi D. Ursodeoxycholic acid improves gastrointestinal motility defects in gallstone patients. World J Gastroenterol. 2006; 12(33): 5336-43.
- Xiao ZL, Biancani P, Carey MC, Behar J. Hydrophilic but not hydrophobic bile acids prevent gallbladder muscle dysfunction in acute cholecystitis. Hepatology. 2003; 37(6): 1442-50.
- Xiao ZL, Rho AK, Biancani P, Behar J. Effects of bile acids on the muscle functions of guinea pig gallbladder. Am J Physiol Gastrointest Liver Physiol. 2002; 283(1): G87-94.
- Kano M, Shoda J, Satoh S, Kobayashi M, Matsuzaki Y, Abei M, Tanaka N. Increased expression of gallbladder cholecystokinin: a receptor in prairie dogs fed a high-cholesterol diet and its dissociation with decreased contractility in response to cholecystokinin. J Lab Clin Med. 2002; 139(5): 285-94.
- van de Heijning BJ, van de Meeberg PC, Portincasa P, Doornewaard H, Hoebers FJ, van Erpecum KJ, Vanberge-Henegouwen GP. Effects of ursodeoxycholic acid therapy on in vitro gallbladder contractility in patients with cholesterol gallstones. Dig Dis Sci. 1999; 44(1): 190-6.
- Mendez-Sanchez N, Brink MA, Paigen B, Carey MC. Ursodeoxycholic acid and cholesterol induce enterohepatic cycling of bilirubin in rodents. Gastroenterology. 1998; 115(3): 722-32.
- Beuers U. Drug insight: Mechanisms and sites of action of ursodeoxycholic acid in cholestasis. Nat Clin Pract Gastroenterol Hepatol. 2006; 3(6): 318-28.
- Pemberton PW, Aboutwerat A, Smith A, Warnes TW. Ursodeoxycholic acid in primary biliary cirrhosis improves glutathione status but fails to reduce lipid peroxidation. Redox Rep. 2006; 11(3): 117-23.
- Jeong HJ, Kim CG. Pretreatment with ursodeoxycholic acid (UDCA) as a novel pharmacological intervention in hepatobiliary scintigraphy. Yonsei Med J. 2005; 46(3): 394-8.
- Gunsar C, Melek M, Karaca I, Sencan A, Mir E, Ortac R, Canan O. The biochemical and histopathological effects of ursodeoxycholic acid and metronidazole on total parenteral nutrition-associated hepatic dysfunction: an experimental study. Hepatogastroenterology. 2002; 49(44): 497-500.
- Das JB, Cosentino CM, Levy MF, Ansari GG, Raffensperger JG. Early hepatobiliary dysfunction during total parenteral nutrition: an experimental study. J Pediatr Surg. 1993; 28(1): 14-8.
- Spier BJ, Pfau PR, Lorenze KR, Knechtle SJ, Said A. Risk factors and outcomes in post-liver transplantation bile duct stones and casts: A case-control study. Liver Transpl. 2008; 14(10): 1461-5.
- Lukivskaya OY, Maskevich AA, Buko VU. Effect of ursodeoxycholic acid on prostaglandin metabolism and microsomal membranes in alcoholic fatty liver. Alcohol. 2001; 25(2): 99-105.
- Bomzon A, Ljubuncic P. Ursodeoxycholic acid and in vitro vasoactivity of hydrophobic bile acids. Dig Dis Sci. 2001; 46(9): 2017-24.
- Ljubuncic P, Said O, Ehrlich Y, Meddings JB, Shaffer EA, Bomzon A. On the in vitro vasoactivity of bile acids. Br J Pharmacol. 2000; 131(3): 387-98.
- Sinisalo J, Vanhanen H, Pajunen P, Vapaatalo H, Nieminen MS. Ursodeoxycholic acid and endothelial-dependent, nitric oxide-independent vasodilatation of forearm resistance arteries in patients with coronary heart disease. Br J Clin Pharmacol. 1999; 47(6): 661-5.
- Pak JM, Adeagbo AS, Triggle CR, Shaffer EA, Lee SS. Mechanism of bile salt vasoactivity: dependence on calcium channels in vascular smooth muscle. Br J Pharmacol. 1994; 112(4): 1209-15.
- Ohtake M, Sandoh N, Sakaguchi T, Tsukada K, Hatakeyama K. Enhancement of portal blood flow by ursodeoxycholic acid in partially hepatectomized rats. Surg Today. 1996; 26(2): 142-4.
- Bomzon A, Ljubuncic P. Bile acids as endogenous vasodilators? Biochem Pharmacol. 1995; 49(5): 581-9.
- Pak JM, Lee SS. Vasoactive effects of bile salts in cirrhotic rats: in vivo and in vitro studies. Hepatology. 1993; 18(5): 1175-81.
- Benedetti A, Alvaro D, Bassotti C, Gigliozzi A, Ferretti G, La Rosa T, Di Sario A, Baiocchi L, Jezequel AM. Cytotoxicity of bile salts against biliary epithelium: a study in isolated bile ductule fragments and isolated perfused rat liver. Hepatology. 1997; 26(1): 9-21.
- Bouscarel B, Ceryak S, Robins SJ, Fromm H. Studies on the mechanism of the ursodeoxycholic acid-induced increase in hepatic low-density lipoprotein binding. Lipids. 1995; 30(7): 607-17.
- Itoh S, Kono M, Akimoto T. Psoriasis treated with ursodeoxycholic acid: three case reports. Clin Exp Dermatol. 2007; 32(4): 398-400.
|