Русский | English
Статьи по онкологии: |
| Меланома |
| Колоректальный рак |
Влияние ксеногенной полиантигенной клеточной вакцины на выживаемость больных с метастатической меланомой III и IV клинической стадией |
|
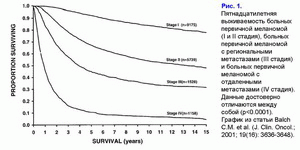
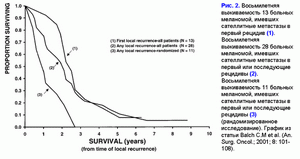
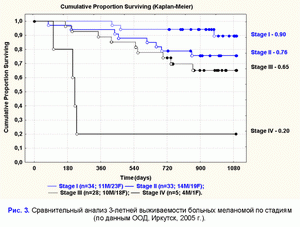
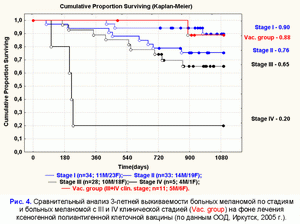
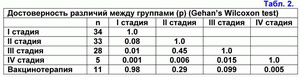
Поделиться ссылкой: Прочитать статью в pdf формате По данным Balch C.M. et al. (J. Clin. Oncol.; 2001; 19(16): 3636-3648) 3-х летняя выживаемость для больных первичной меланомой с I стадией составляет 98%, со II стадией - 77%, с III стадией - 55%, с IV стадией - 15% (рис. 1). Появление сателлитных или транзиторных или отдаленных метастазов меланомы значительно сокращает выживаемость больных меланомой (рис. 2). По данным Balch C.M et al. (An. Surg. Oncol.; 2001; 8: 101-108) после появления первых сателлитных или транзиторных метастазов меланомы 3-х летняя выживаемость для больных меланомой составляет только 30%, после появления повторных сателлитных или транзиторных или отдаленных метастазов меланомы уже 2-х летняя выживаемость составляет только 20%, 3-х летней - нет (рис. 2). Цель: изучить влияние ксеногенной полиантигенной клеточной вакцины на выживаемость больных метастатической меланомой с III и IV клинической стадией. Материалы и методы: Контрольную группу составили 111 больных первичной меланомой, пролеченных в период с 01.01.2001 г. по 25.04.02 г.: I стадия - 34 больных (11М/23Ж; средний возраст - 54±15); II стадия - 33 больных (14М/19Ж; средний возраст - 54±15); III стадия - 28 больных (10М/18Ж; средний возраст - 53±147); IV стадия - 5 больных (4М/1Ж; средний возраст - 52±7). Группу больных метастатической меланомой с III и IV клинической стадией, прошедших курс лечения ксеногенной полиантигенной клеточной вакцины, составили 11 больных (4М/7Ж; средний возраст - 53±13). В эту группу больных были включены больные с метастатической меланомой с III и IV клинической стадией: 6 больных с III клинической стадией (все были прооперированы - или перед вакцинацией или на фоне проведения вакцинации) и 5 больных с IV клинической стадией. Ответную реакцию на вакцинотерапию оценивали по стандартным критериям ВОЗ. Распределение выживаемости оценивали с помощью метода Kaplan-Meier. Результаты: 3-х летняя выживаемость для контрольной группы больных меланомой с I стадией составила 90%, со II стадией - 76%, с III стадией - 65%, с IV стадией - 20% (рис. 3).3-х летняя выживаемость больных первичной меланомой, пролеченных в ИООД, значимо не отличается от выживаемости больных меланомой, пролеченных в онкологических центрах США (табл. 1). Стандартные методы лечения первичной меланомы (хирургические, химиотерапевтические и другие) значимо не влияют на 3-х летнюю выживаемость. Выживаемость для больных, прошедших курс вакцинотерапии, рассчитывали от первичной даты постановки диагноза. 3-х летняя выживаемость для больных с метастатической меланомой с III и IV клинической стадией составила 88% (рис. 4). Транзиторные и/или отдаленные метастазы у данной группы больных возникли в среднем через 404±208 дней от первичной даты постановки диагноза. Вакцинотерапия больных с метастатической меланомой c III и IV клинической стадией с использованием ксеногенной полиантигенной клеточной вакцины способствует достоверному увеличению 3-х летней выживаемости больных (табл. 2). Частичная регрессия отмечена у 3-х больных, послеоперационная ремиссия - у 4-х больных, прогрессия заболевания - у 4-х больных. У последней группы больных выявлено замедление скорости прогрессии и, как следствие, увеличение продолжительности выживаемости (табл. 3). На фоне проводимого лечения 2 больных умерли от прогрессии заболевания в сроки 208±80 дней от начала вакцинации. Эти больные к моменту начала курса вакцинотерапии уже имели 3-ий или 4-ый рецидив меланомы. Выводы: Предварительные результаты, показывают, что вакцинотерапия больных с метастатической меланомой с использованием ксеногенной полиантигенной клеточной вакцины способствует уменьшению риска возникновения рецидива (послеоперационной ремиссии) или частичной регрессии, что способствует достоверному увеличению выживаемости больных. Список литературы:
|
|
|